1 前 言
药物是一种特殊商品,凡是涉及用于药物的原料、辅料、包装材料、诊断试剂、试验动物,以及制药环境、药检仪器等,都必须符合G家药典及有关规定。药物溶出度是指药物在规定介质中,在一定条件下从片剂或胶囊等固体制剂中溶出的速度和溶出的程度。药物溶出度直接影响药物在体内的吸收和利用,是评价药物质量的一个内在指标。在药物生产检验、临床疗效考察、药品稳定性检验、新药研制、处方筛选、工艺改进[1~8 ]等许多方面都要考察这一指标。无论美G、英G、中G还是日本,药物溶出度检查实际是指药物固体制剂按照各G药典规定的方法,在一定时间内从固体制剂溶入介质的累计百分率(以被测试剂标示量计算) 。中G药典(2000 年版) 规定,片剂或硬胶囊制剂45min 的溶出度应大于70 %。一般认为下列药物,必须测定溶出度:(1) 难溶或难吸收的药物;(2) 治疗量与中毒量接近的药物;(3) 要求缓释、控释或长效的药物;(4) 用于治疗严重疾病的药物;(5) 急救、抢救用的药物。药物溶出度检查是评价制剂品质和工艺水平的一种有效手段,也是评价制剂活性成分生物利用度和制剂均匀度的一种有效标准,能有效区分同一种药物生物利用度的差异,因此是制药工业质量控制必检项目之一。从理论上讲,药物的体内试验(包括体内药物动力学的研究和临床试验) 才是评价药物**根本和**可靠的依据。20 世纪80 年代以来,生物利用度成为衡量药品质量的一个重要参数,但生物利用度实验工作量大、成本高,从药物生产的实际情况来看,不可能对每一个药物样品都采用体内实验来筛选评定。药物溶出度检查是一种模拟口服固体制剂在胃肠中溶出过程的体外实验法。尽管体内
检验和体外检验结果不会完全一致,但具有一定相关性[1 ,9~12 ] ,而且溶出度的体外检验较体内检验简单易行,仍不失为一个经济有效的质量检测、控制手段。本文较系统地综述了G内外药物溶出度检查方法与仪器的发展现状,及可能的发展趋势。
2 药物溶出度检查方法
溶出度检查装置一般由模拟胃和检测装置两部分构成。模拟胃是一种程序控温的药物溶解装置,用以模拟胃中的环境,通常控制温度为37 ℃,酸度大小随药物的不同而不同。根据溶解装置的不同,溶出度检查方法有桨状搅拌器法、转篮法、流通池法 (flow2through apparatus) 、桨碟法(paddle over disk) 、中池法(cell method)、转筒法(cylinder) 和小杯法等。我G药典把溶出度检查方法分为转篮法、桨状搅拌器法和小杯法。我G药典2000 年版收载的转篮法、桨状搅拌器法检测装置与美G药典和英G药典收载的相应装置一致[13 ] ; 小杯法是具有中G特色的方法,实际为缩小容积的桨状搅拌器法。转篮法、桨状搅拌器法以及小杯法是通过搅拌或旋转在介质中产生强制对流进行混合。转篮法的主要缺点是网篮或过滤装置都可能发生堵塞,桨状搅拌器法的明显缺点是样品可能上浮;采用转篮法和桨状搅拌器法,溶解度低而剂量大的药物往往会在溶出液中迅速达到饱和状态,因此很难测出其溶出度。G外一些药典还收录了流通池法、桨碟法、转筒法和中池法等其他方法。其中,流通池法能使样品一直暴露在均匀无旋涡的新鲜介质中,适用于难溶性药物的溶出度检查; 在测试中还可以改变pH条件,使测试参数符合生理条件,比转篮法和桨状搅拌器法能更好地模拟药物在体内的转运过程[14 ] ,是现行药典溶出度检查方法的补充和完善。
3 药物溶出度检查仪器
目前常用的智能
溶出仪系列,能进行准确的温度控制,转篮或搅拌桨的转速可以任意调节,采用单片机技术测量实际转速,时间可以自动预置。我G比较常用的药物
溶出仪是天津大学无线电厂生产的ZRS - 8G型和D - 800 型智能药物
溶出仪。这两种仪器的转速分辨率为1 r/ min ,测温分辨率0. 1 ℃,各方面性能均可达到G家药典的标准。该厂开发研制的ADUV8 型药品溶出取样紫外分析检测系统,可进行全封闭在线工作;八通道蠕动泵可自动取样、回液,多点取样时无须补液;专门设计的双光束紫外分光光度计具有八连池样品测试功能,可对8 个样品进行快速、连续测定,并可通过选配不同光程的石英流通池(0. 5cm ,0. 2cm ,0. 1cm) ,实现2 、5 、10 倍稀释。在美G,很多药厂采用Beckman 公司的Du - 60系列紫外监测自动溶出仪,Waters 公司和Hanson公司合作开发的高效液相色谱定量自动溶出仪。使用Du - 60 系列自动溶出仪的整个溶出实验都是自动进行的,仪器使用方便、省时、可靠。Waters 公司和Hanson 公司合作开发的高效液相色谱自动溶出仪系统能将多种成分分离,避免了有效成分光谱的互相干扰和辅料成分光谱的干扰,所以很受欢迎。
G外还有一种带半透膜的溶出仪[15 ] ,如荷兰Lab2CAT 公司的PTSWO 溶出仪,能更好地模拟药物在人体肠胃中的吸收过程。常用的检测器有紫外- 可见分光光度计和高效液相色谱仪。近年来,G外又推出一种反射光谱定量检测器,如美GDelphian 公司的Rainbow 检测器[16~18 ] 。这种检测器有一个特殊设计的探头,探头能发射激光,同时又能接收经过规定距离(光程)后反射回来的反射光。反射光经光纤传**仪器的光电池,根据出射光和反射光强度的不同可计算溶液的浓度。使用Rainbow 检测器时,可以把探头直接插入溶解装置进行实时监测,不用把样品取出放入紫外- 可见分光光度计,避免了取样带来的误差。Rainbow 检测器在原理上属于紫外- 可见光检测器,不同的是,使用紫外- 可见分光光度计时,在取样管和流通池中是溶有样品的溶液,而使用Rain2bow 检测器时,只有光纤中光的传输。
4 检测结果判断
药物溶出度检测仪器装有6 套模拟胃装置,可供6 份样试同时检测溶出度。每个药片的溶出量,按标示含量计算,6 片均应不低于规定值(Q) ;除另有规定外,Q 为标示含量的70 %。如6 片中仅有1~2 片低于规定值,但不低于Q - 10 % ,且平均溶出量不低于规定值,仍可判定为符合规定。如6 片中有1~2 片低于Q - 10 % ,应另取6 片复试;如初、复试的12 片中仅有2 片低于Q - 10 % ,且平均溶出量不低于规定值,亦可判为符合规定。如供试品的取用量为2 片或2 片以上,每片的平均溶出量,均不低于规定值(Q) ,则可不再复试[19 ] 。
5 干扰因素及其消除措施
药物溶出度检测在实际应用中存在的主要干扰因素有氧气的存在,药物微小颗粒,波长偏差,药物在溶出仪上的吸附效应等。
5. 1 氧气的影响及消除
在搅拌过程中,氧气会产生气泡,影响固体制剂的溶出度[20 ,21 ] 。因此,必须排除介质中的氧气。脱气的方法有多种[22 ,23 ] ,常用的方法是,把介质加热**45 ℃,同时缓慢搅拌,然后在真空条件下过滤,快速搅拌5min。然而,在把介质转移**药物溶解装置的过程中,往往也会引入大量氧气。在这个过程中,介质中的含氧量会增加到原来的275 %[24 ] 。**近美G有人制成空心搅拌桨,从空心搅拌桨中通入氦气,达到排除氧气的目的。该装置附有一个三通阀,空心搅拌杆可用来取样[25 ] 。除氧该装置的结构如图1 所示。
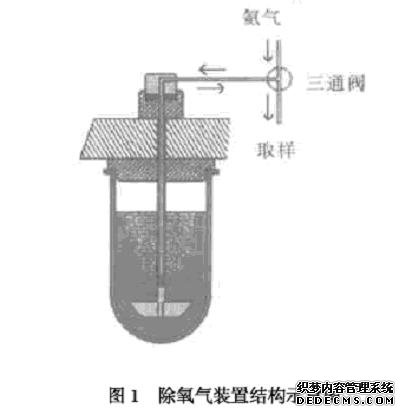
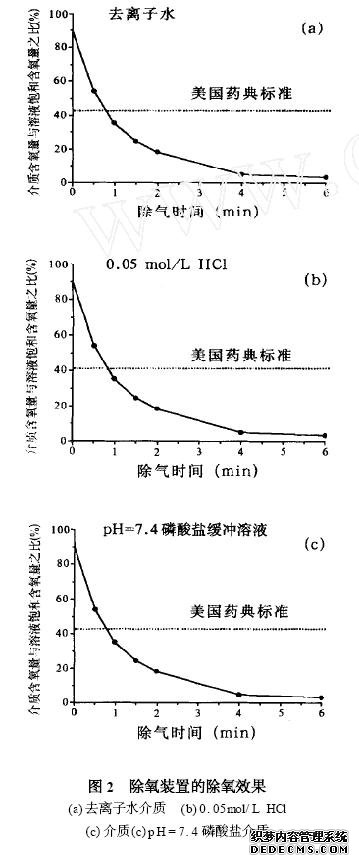
实验表明,处理后介质的氧气含量明显下降。实验所用三种介质为去离子水、0. 05mol/ L HCl 和
磷酸盐缓冲溶液(pH = 7. 4) 。将三种介质分别放入溶解装置, 然后通入氦气, 在37 ℃、搅拌浆转速100rpm 条件下,通气6min。除氧装置的除氧效果如图2 所示。这种方法适用于各类介质,氦气使用量很低,只要1min 就可达到美G药典的要求,有望得到广泛应用。
5. 2 药物微小颗粒的影响及消除
若在被检测溶液中存在微小颗粒,光通过时会产生散射现象,从而使测量结果偏高(即出现正误
差) 。使用普通的紫外- 可见光检测器时,可在取样管端口连接一个双层过滤器(约0. 8μm 和0. 5μm) ,以滤去被检测溶液中的微小颗粒,大大降低溶液对光的散射低。使用Rainbow 检测器时,可使用基线校正方法消除正误差。具体方法是,在药品**大吸收波长处测量一吸收值,再在另一波长处测量基体的吸收值,计算两者之差。
5. 3 波长偏差的影响及消除
中G药典对仪器的波长准确度未作具体规定,但规定试样的测量波长与**大吸收波长允许的误差仅为2nm[26 ] 。使用高效液相色谱法时,分离后用紫外- 可见光检测器检测,所用单色光的波长与**大吸收波长的偏差一般为6~10nm ,这会在一定程度上增加噪声,因此应当使用高精确度、高准确度和高灵敏度的紫外- 可见分光光度计作为高效液相色谱仪的检测装置。
5. 4 药吸附效应的影响及消除
药物在溶解装置或过滤器上有少量吸附,会使测量结果偏低。因此,在实验前必须洗净溶解装置,并确保其无划痕。过滤器上的吸附也影响测量结果,可以采用反冲的方法[27 ]加以消除。
6 药物溶出度检查的发展趋势
各G药典20 世纪70 年代以后相继引入药物溶出度检查。几十年来,药物溶出度检查方法与仪器已取得很大进展[28 ] ,尤其是80 年代以来,随着计算机技术、传感器技术和其他高新技术的发展,溶出度检查技术有了更大的飞跃。目前的发展方向主要是研制高灵敏度、快速、自动、简便、经济的药物溶出度检测仪器和方法,而自动化是其发展的主要趋势。
参考文献
1 祝莉莎,孙殿甲. 中G药学杂志,2000 ,35 (11) :750
2 宗红心,赵钰,李竞. 中G药学杂志,2000 ,35 (2) :110
3 赵瑞芝,欧润妹,袁小红. 中G药学杂志,2001 ,36 (2) :101
4 周宇,蒋雪涛,周建标等. 中G药学杂志,2001 ,36 (10) :
673
5 李凤前,胡晋红,朱全刚等. 中G药学杂志,2002 ,37 (2) :
461
6 吕竹芬,谭载友,张蜀等. 2000 ,17 (6) :461
7 高声传,郭涛,陈济民等. 中G医院医学杂志,2001 ,21
(3) :133
8 樊宏伟,乔亚闲,程彦文等. 哈尔滨医科大学学报,2000 ,
34 (3) :223
9 李凤前,陆彬,陈文彬. 中G药学杂志,2001 ,36 (7) :458
10 吴琳华,付红焱,刘红梅等. 中G药学杂志,2001 ,36 (6) :
397
11 黄小玲,黄东亮. 中G药业,2000 ,9 (3) :27
12 张立超,胡晋红,李珍等. 上海医院药学,2000 ,11 (1) :13
13 许鸣镝,胡琴. 中G药学杂志,2000 ,35 (7) :491
14 殷恭宽. 物理药学. 北京:北京医科大学中G协和医科大
学联合出版社11993 ,292.
15 张霖泽,**兰勤,Narnit H S. 中G药学杂志, 1995 , 30
(6) :366
16 Aldridge P K, Koskteck L J . Dissolution Technologies ,
1995 ,2 (4) :10
17 Bynum K C , Kraft E , Pocreva J et al. Dissolution Tech2
nologies ,1999 ,6 (4) :3
18 Bynum K, Kassis A , Gehrlein L , Palermo P. Application
and Validation of a U. V Fiber Optic Dissolution System.
Dissolution Testing Conference ,Philadelphia ,PA ,2001
19 中G药典2001 年版增订本
20 Hanson W A. Hansonbook of Dissolution Testing. Eugene
Oregon :Aster Publishing Corporation ,1991
21 USP. XXIV. 1943
22 马学文. 现代药品检验学. 北京: 人民军医出版社会,
23 Griffith M E ,Curly T E , Martin G P. Dissolution Tech2
nologies ,1997 ,4 (1) :16
24 Diebold S M ,Dressman J B. Pharm Ind ,1998 ,60 :354
25 Schatz C ,Ulmschneider M ,Altermatt R , Marrer S. Disso2
lution Technologies , 2000 ,7 (1) :20
26 孙G新. 分析测试仪器通讯,1997 ,7 (3) :150
27 Liu X Z ,Fang Z L. Anal Chim Acta ,1998 ,358 :103
28 Hanson R. Dissolution : Passt Present & Future . FDA
Workshop ,Philadelphia ,PA , 1996

