口服剂型仍然是患者可用的zui灵活和有效的治疗方法之一。溶出度测试是所有固体口服剂型的要求,并且在整个开发生命周期中用于产品释放和稳定性测试。它是用于检测活性药物成分和配制产品的物理变化的关键分析测试。在药物开发过程的早期阶段,体外溶出度测试支持从给定制剂中优化药物释放。
口服剂型的有效性取决于药物在被吸收到循环中之前溶解在胃肠道液体中的内在能力。因此,片剂或胶囊的溶出速率对该过程是关键的。
药物开发中遇到的关键问题之一是需要优化身体可用的药物水平以获得其所需的治疗效果。在治疗窗外的这种不正确的优化可能潜在地导致生物利用度不足(因此缺乏功效)或相反地,生物利用度太高,从而对患者产生不希望的不良毒性作用。
为了有助于剂型优化,溶出度测试是用于测量给定剂型的药物释放速率的标准化方法。
尽管是制药和生物制药行业中常用的测试,但溶出测试的基本原理往往得不到正确理解。该测试必须具有稳健性和可重复性,能够检测产品性能的任何关键变化,即区分不同的配方和/或批次。
所用的确切溶出技术由剂型特征和预期的给药途径决定。对于固体剂型,工业标准溶出测试方法是美G药典(USP)装置I(篮子)和USP装置2(桨叶)。立即,改良和延长释放通常在具有USP 2桨的标准溶解浴中进行测试。对于易于漂浮的口服剂型,通常需要USP 1(篮子)。除了上述设备类型之外,还有其他技术可用,例如USP 3(往复式汽缸),USP 4(流通式电池),USP 5(桨式换盘),USP 6(汽缸)和USP 7。 (往复式支架)。
在开发溶出仪过程方面,需要评估几个方面以实现稳健的方法。必须评估设备类型,介质和搅拌速率等因素,并且这些因素应适合于所测试的产品。出于本文的目的,将讨论zui常见的技术(USP设备1和2),包括在开发溶出方法时应考虑的典型方法参数的概述。
为了使剂型有效,必须提取API(溶解在溶液中)然后吸收到体循环中以促进其转运到活性部位。该过程影响API的总体生物利用度。了解这一过程是进行体外方法开发的基础。溶解是将API从固体剂型提取到溶液中的过程。下面给出了一个简单的图示:
图1:一个固体口服剂型的溶出
一旦API处于溶液中,就可以发生吸收过程,由此药物物质从胃肠腔进入循环系统,然后它可以进入相关的受体部位以发挥生物反应。
溶出度是一种体外测试,用于评估API如何从固体剂型中提取。它可以提供体内溶出效率的指示,但jue不提供任何药物吸收的数据。为了评估后者,需要产生药代动力学数据并用于补充溶出工作。
如果选择合适的体外条件并进行适当评估(以模拟体内条件),它可以帮助确定成功的体外 - 体内相关性(IVIVC),或者zui坏的情况下,确定两者之间的关系。应该注意的是,对于QC目的而言zui佳的溶出参数可能不适合建立IVIVC,因此可能需要两次溶出试验以满足开发和监管需求。
在开发溶出方法时,重要的是对该过程采取合理的系统方法,并确保牢记科学和监管原则。稳健的溶出方法应该没有明显的干扰(例如由赋形剂引起的基质效应),产生低的可变性(精确度)并产生良好的轮廓形状。该方法还应该受到挑战,以区分具有不同质量属性的批次材料。一旦确定合适的培养基和装置的过程完成,就需要进一步优化该方法以评估培养基的离子强度,搅拌速率和(如果需要的话)表面活性剂浓度。zui终开发的方法应该能够区分不同的配方/批次,但仍保持可接受的精度和稳健性。关于精确度,早期和晚期时间点的典型限制将分别<20%和<10%RSD。

图2:典型的溶解浴装置
水槽条件
沉降条件定义为“溶液浓度通常对应于溶解介质中API的标称工作浓度的5-10倍”。确定水槽的实现对于建立合适的溶解方法至关重要。如果不能实现这些(并且因此介质达到饱和点),则不能始终如一地测量溶解速率。重要的是,在进行溶出试验时,对结果的**影响应该是产品的搅拌速率和溶解度。
媒体
筛选潜在培养基时的zui初焦点是从水基的那些开始,在推荐的离子强度的1.2-6.8的pH范围内(根据USP / EP)。当评估在整个pH范围内在水性介质中显示低溶解度的API时,建议加入表面活性剂,尽管使用的水平应尽可能低。
剂型
在方法开发阶段,应考虑剂型类型(胶囊,片剂等),强度,赋形剂,释放类型(即时,持续,延迟),稳定性数据和表面涂层的基本特征。此外,制造变量对于评估不同配方之间API释放的差异也是关键。完善的溶出方法应该允许区分各种产品属性。
进行溶解时,将在设定的时间点取出样品,并绘制相对于时间的溶解百分比(如下图3所示):
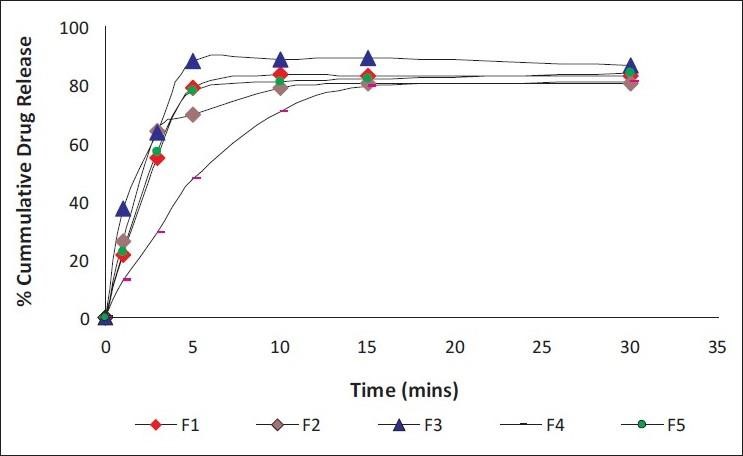
图3:不同制剂之间溶出曲线表示歧视
在溶出度分析的整个过程中,确保维持目视观察至关重要。这可以提供额外的数据来支持分析结果中的任何数量差异。
需要建立溶解的分析结果。在可能的情况下,为了保持简单性和效率(并假设存在合适的发色团),可以采用简单的UV涂饰; 这也需要获得合适的特异性以确保活性物质的吸光度不受任何其他干扰的影响。
通常,使用HPLC-UV进行定量。这通常是有利的,以便减少/消除可能以其他方式损害独立UV方法的干扰。另外,通过缩短运行时间以允许溶出分析所需的高样品通量,很可能先前的HPLC测定方法适用于溶出样品。HPLC还提供了调节进样体积的灵活性,以适应不同产品强度可能需要的样品浓度变化。
在某些情况下,它可能是筛选材料的元素组分的实际替代品,例如对于活性材料是无机盐的产品,或者在传统检测有问题的情况下,则可以监测计数器取而代之的是钠或钙等离子。
有许多元素光谱技术可用于此目的。仪器的选择取决于所需的分析物和溶液中的预期浓度。
例如,溴化钾片剂的溶出曲线可以通过使用火焰原子吸收光谱法(FAAS)来测量钾的水平,或者溴化物的浓度(以元素溴测量)可以通过电感耦合等离子体质量来测量。光谱法(ICP-MS)。另一个应用可能是使用电感耦合等离子体 - 光学发射光谱(ICP-OES)来确定从富马酸亚铁片溶出的溶液中铁的含量
总之,合适的溶出程序的设计必须考虑到API,配方和分析方法的许多参数。体外溶出度测试应提供强大的数据体,以确保产品性能和质量。在整个过程中,重要的是确保体外溶出类似于体内条件。如果有效地设计溶出程序,它将加速药物开发,并且理想地减少对人类研究的需要。